京都大学iPS细胞研究所(CiRA)于2021年12月8日宣布,开发出了一种可用于基因组编辑治疗的脂质纳米颗粒(LNP)运输系统,并成功编辑了肌肉萎缩症小鼠的基因组。这是与武田制药株式会社联合研究项目“T-CiRA”的成果。
杜兴氏肌肉萎缩症是一种顽固的肌肉疾病,由一个阻止产生肌营养蛋白的基因的部分突变引起。 基因组编辑疗法能使肌营养蛋白的生产成为可能,有望成为这种疾病的治疗方法。
然而,由于该疾病影响骨骼肌的广泛区域,单剂量的基因组编辑药物将是不够的,需要多剂量。 然而,使用腺相关病毒(AAV)载体的传统基因转移方法会产生中和性抗体,使重复基因转移变得困难。
该团队现在已经开发出一种方法,利用LNP(脂质纳米粒)将CRISPR-Cas9(一种基因组编辑所需的酶)输送到广泛的肌肉组织。
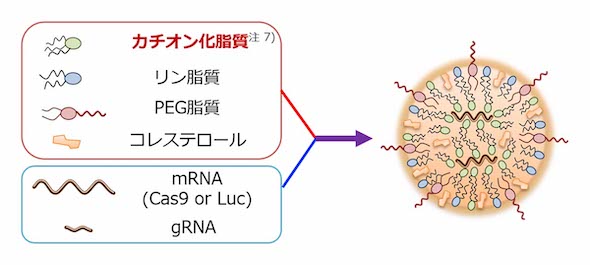
首先,他们寻找一种能有效传递mRNA的LNP成分。 这里发现的LNP加载了Cas9 mRNA和向导RNA(LNP-CRISPR),并证实在小鼠骨骼肌中有效地发生基因组编辑。
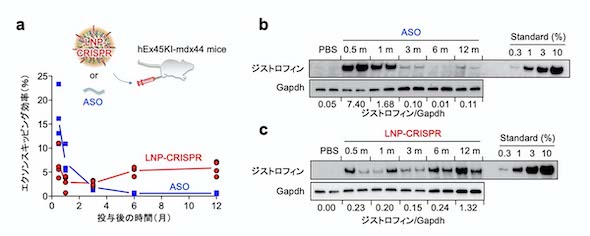
对肌肉萎缩症的小鼠施以单剂量的LNP-CRISPR,肌营养蛋白的恢复持续了12个月。 传统的核酸药物,作用于肌营养蛋白基因的mRNA,只能持续一个月。
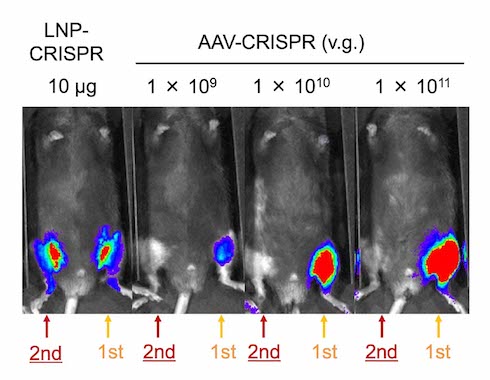
当第一次用药28天后再次用药时,基因组编辑活性得到确认。 此外,在一个肌肉萎缩症的小鼠中,在两周的时间里接受了6次的LNP-CRISPR,在38.5%的肌肉纤维中观察到了肌营养蛋白的表达。 这表明,通过重复使用LNP-CRISPR可以进行基因组编辑。
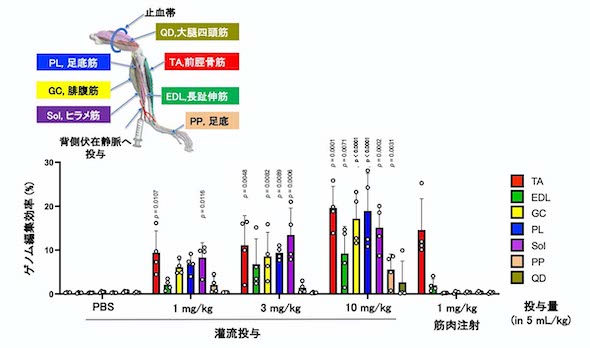
为了找出如何有效地将药物输送到更广泛的肌肉区域,研究人员比较了静脉灌注与肌肉注射的基因组编辑程度。 通过肌肉注射,基因组编辑只发生在被注射的骨骼肌中,而通过静脉灌注,基因组编辑则发生在众多肌肉中。
对于肌肉萎缩症的基因组编辑,有必要开发一种将基因组编辑酶扩散到整个骨骼肌组织的方法。 这项新技术具有长效性,可以反复给药,有望成为治疗骨骼肌疾病的新方法。
本网系信息发布平台,仅提供信息存储服务,如有转载、侵权等任何问题,请联系管理员(yiliaojiankangtoutiao@gmail.com )处理。
文章评论